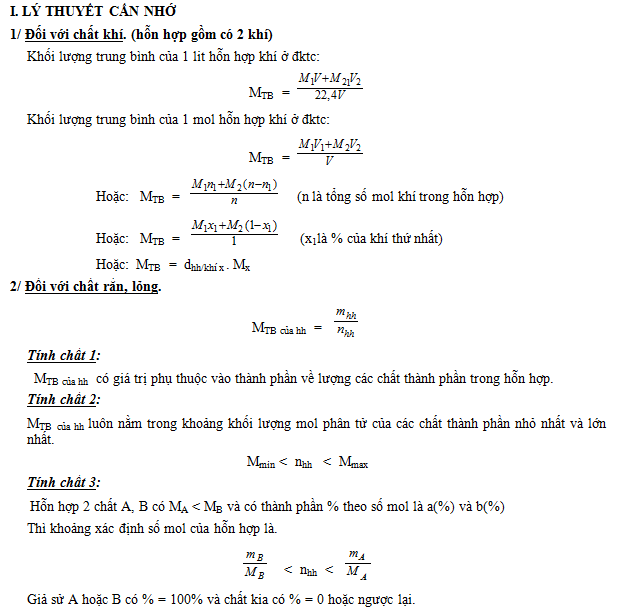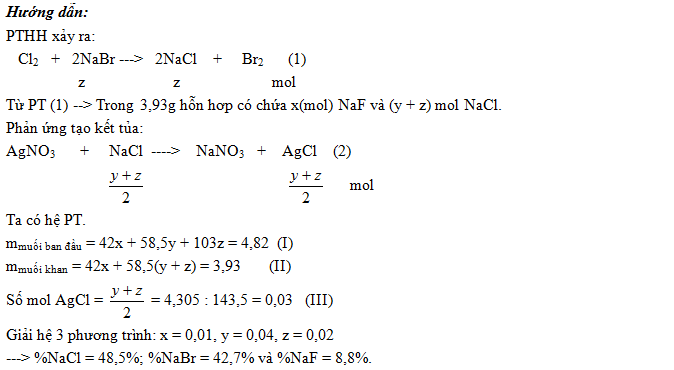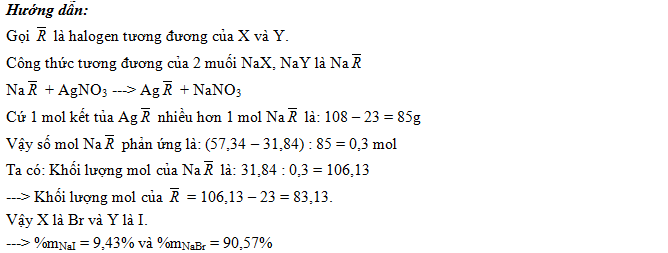Dạng toán muối halogen (Nâng cao)
Muối halogen hay còn gọi là muối của các nguyên tố nhóm VII có những tính chất gì, dạng bài tập đặc trưng ra sao.
Mời các bạn học sinh tham khảo thêm:
50 câu trắc nghiệm (LT + BT) chương kim loại
Bài viết dưới đây sẽ giúp học sinh trả lời câu hỏi trên. Đồng thời giới thiệu một số phương pháp giải bài tập nâng cao về muối halogen
TOÁN HỖN HỢP MUỐI HALOGEN (NHÓM VII)
Các bài toán vận dụng số mol trung bình và xác định khoảng số mol của chất.
Cần nhớ:
halogen đứng trên đẩy được halogen đứng dưới ra khỏi muối.
Tất cả halogen đều tan trừ: AgCl, AgBr, AgI.
Hiển nhiên: AgF tan.

Dạng toán muối halogen (Nâng cao)
II. BÀI TẬP VẬN DỤNG
Bài 1: Một hỗn hợp 3 muối NaF, NaCl, NaBr nặng 4,82g. Hoà tan hoàn toàn trong nước được dung dịch A. Sục khí Cl2 vào dung dịch A rồi cô cạn, thu được 3,93g muối khan. Lấy một nửa lượng muối khan này hoà tan trong nước rồi cho phản ứng với dung dịch AgNO3 dư, thu được 4,305g kết tủa. Viết các phản ứng xảy ra và tính thành phần % theo khối lượng mỗi muối trong hỗn hợp ban đầu.
Bài 2: Dung dịch A có chứa 2 muối là AgNO3 và Cu(NO3)2, trong đó nồng độ của AgNO3 là 1M. Cho 500ml dung dịch A tác dụng với 24,05g muối gồm KI và KCl, tạo ra được 37,85g kết tủa và dung dịch B. Ngâm một thanh kẽm vào trong dung dịch B. Sau khi phản ứng kết thúc nhận thấy khối lượng thanh kim loại kẽm tăng thêm 22,15g.
a/ Xác định thành phần % theo số mol của muối KI và KCl.
b/ Tính khối lượng Cu(NO3)2 trong 500ml dung dịch A.
Đáp số:
a/ nKI = nKCl —> %nKI = %nKCl = 50%.
b/ Số mol Cu(NO3)2 = 0,5 mol —-> khối lượng Cu(NO3)2 = 94g.
Bài 3: Hoà tan 5,94g hỗn hợp 2 muối clorua của 2 kim loại A và B( A, B là 2 kim loại thuộc phân nhóm chính nhóm II) vào nước, được 100ml dung dịch X. Người ta cho dung dịch X tác dụng vừa đủ với dung dịch AgNO3 thì thu được 17,22g kết tủa. Lọc kết tủa thu được dung dịch Y có thể tích là 200ml. Cô cạn dung dịch Y thu được m(g) hỗn hợp muối khan.
a/ Tính m?
b/ Xác định CTHH của 2 muối clorua. Biết tỉ lệ KLNT A so với B là 5 : 3 và trong muối ban đầu có tỉ lệ số phân tử A đối với số phân tử muối B là 1 : 3.
c/ Tính nồng độ mol/l của các muối trong dung dịch X.
Hướng dẫn:
Viết các PTHH xảy ra.
Đặt x, y là số mol của muối ACl2 và BCl2
Ta có: (MA + 71).x + (MB + 71)y = 5,94
Số mol AgCl tạo ra = 2(x + y) = 17,22 : 143,5 = 0,12 mol —> x + y = 0,06.
—-> xMA + yMB = 1,68
dd Y thu được gồm x mol A(NO3)2 và y mol B(NO3)2 —> muối khan.
(MA + 124)x + (MB + 124)y = m
Thay các giá trị ta được: m = 9,12g
b/ theo bài ra ta có:
MA : MB = 5 : 3
x : y = nA : nB = 1 : 3
x + y = 0,06
xMA + yMB = 1,68
Giải hệ phương trình ta được: MA = 40 và MB = 24.
Nồng độ mol/l của các dung dịch là:
CM(CaCl2) = 0,15M và CM(BaCl2) = 0,45M.
Bài 4: Chia 8,84 gam hỗn hợp MCl và BaCl2 thành 2 phần bằng nhau. Hoà tan phần 1 vào nước rồi cho phản ứng với AgNO3 dư thu được 8,61g kết tủa. Đem điện phân nóng chảy phần 2 đến hoàn toàn thu được V lit khí X ở đktc. Biết số mol MCl chiếm 80% số mol trong hỗn hợp ban đầu.
a/ Xác định kim loại M và tính thành phần % theo khối lượng mỗi chất trong hỗn hợp đầu.
b/ Tính V?
Hướng dẫn:
Gọi số mol MCl và BaCl2 trong 8,84g hỗn hợp là 2x và 2y (mol)
Các PTHH xảy ra:
MCl + AgNO3 —> AgCl + MNO3
BaCl2 + 2AgNO3 —-> Ba(NO3)2 + 2AgCl
Phần 2:
2MCl —–> 2M + Cl2
BaCl2 ——> Ba + Cl2
Ta có: nAgCl = x + 2y = 8,61 : 143,5 = 0,06 mol
—> nCl = (x + 2y) : 2 = 0,03 mol
Vậy thể tích khí Cl2 thu được ở đktc là:
V = 0,03 . 22,4 = 0,672 lit
– Vì MCl chiếm 80% tổng số mol nên ta có: x = 4y —> x = 0,04 và y = 0,01.
mhh X = (M + 35,5).2x + (137 + 71).2y = 8,84 —> M = 23 và M có hoá trị I, M là Na.
%NaCl = 52,94% và %BaCl2 = 47,06%.
Bài 5: Một hợp chất hoá học được tạo thành từ kim loại hoá trị II và phi kim hoá trị I. Hoà tan 9,2g hợp chất này vào nước để có 100ml dung dịch. Chia dung dịch này thành 2 phần bằng nhau. Thêm một lượng dư dung dịch AgNO3 vào phần 1, thấy tạo ra 9,4g kết tủa. Thêm một lượng dư dung dịch Na2CO3 vào phần 2, thu được 2,1g kết tủa.
a/ Tìm công thức hoá học của hợp chất ban đầu.
b/ Tính nồng độ mol/l của dung dịch đã pha chế.
Hướng dẫn.
Đặt R là KHHH của kim loại hoá trị II và X là KHHH của phi kim có hoá trị I
Ta có CTHH của hợp chất là: RX2
Đặt 2a là số mol của hợp chất RX2 ban đầu.
Ta có: 2a(MR + 2MX) = 9,2 (g) —-> a.MR + 2.a.MX = 4,6 (I)
Viết các PTHH xảy ra:
Phần 1: 2a(MAg + MX) = 216.a + 2.a.MX = 9,4 (II)
Hay 2.a.MAg – a.MR = 216.a – a.MR = 9,4 – 4,6 = 4,8 (*)
Phần 2: a(MR + MCO) = a.MR + 60.a = 2,1 (III)
Hay 2.a.MX – a.MCO = 2.a.MX – 60.a = 4,6 – 2,1 = 2,5 (**)
Từ (*) và (III) —> 216.a + 60.a = 4,8 + 2,1 = 6,9 —> a = 0,025.
Thay a = 0,025 vào (III) —> MR = 24. Vậy R là Mg
Thay vào (I) —> MX = 80. Vậy X là Br.
CTHH của hợp chất: MgBr2
Đáp số:
a/ Công thức hoá học của hợp chất là MgBr2
b/ Nồng độ dung dịch MgBr2 là 0,5M.
Bài 6: Hỗn hợp A gồm 3 muối MgCl2, NaBr, KI. Cho 93,4g hỗn hợp A tác dụng với 700ml dung dịch AgNO3 2M. Sau khi phản ứng kết thúc thu được dung dịch D và kết tủa B, cho 22,4g bột Fe vào dung dịch D. Sau khi phản ứng xong thu được chất rắn F và dung dịch E. Cho F vào dung dịch HCl dư tạo ra 4,48 lit H2 (đktc). Cho dung dịch NaOH dư vào dung dịch E thu được kết tủa, nung kết tủa trong không khí cho đến khối lượng không đổi thu được 24g chất rắn. Tính khối lượng kết tủa B.
Hướng dẫn:
Gọi a, b, c lần lượt là số mol MgCl2, NaBr, KI.
Viết các PTHH xảy ra.
Dung dịch D gồm: Mg(NO3)2, NaNO3, KNO3, và AgNO3 còn dư.
Kết tủa B gồm: AgCl, AgBr, AgI.
Rắn F gồm: Ag và Fe còn dư.
Dung dịch E: Fe(NO3)2, Mg(NO3)2, NaNO3, KNO3 chỉ có Fe(NO3)2, Mg(NO3)2 tham gia phản ứng với dung dịch NaOH dư.
—-> 24g rắn sau khi nung là: Fe2O3 và MgO. Đáp số: mB = 179,6g.
Bài 7: Hoà tan 104,25g hỗn hợp các muối NaCl và NaI vào nước. Cho đủ khí clo đi qua rồi đun cạn. Nung chất rắn thu được cho đến khi hết hơi màu tím bay ra. Bả chất rắn thu được sau khi nung nặng 58,5g. Tính thành phần % theo khối lượng mỗi muối trong hỗn hợp.
Hướng dẫn:
Gọi a, b lần lượt là số mol của NaCl và NaI
Khi sục khí clo vào thì toàn bộ muối NaI chuyển thành muối NaCl.
Tổng số mol muối NaCl sau phản ứng là: (a + b) = 58,5 : 58,5 = 1 mol
và ta có: 58,5a + 150b = 104,25
Giải phương trình ta được: a = 0,5 và b = 0,5
—> %mNaCl = (58,5 . 0,5 : 104,25 ) . 100% = 28,06%
và %mNaI = 100 – 28,06 = 71,94%
Bài 8: Cho 31,84g hỗn hợp NaX và NaY (X, Y là hai halogen thuộc 2 chu kì liên tiếp) vào dung dịch AgNO3 có dư thu được 57,34g kết tủa. Tìm công thức của NaX và NaY và thành phần % theo khối lượng của mỗi muối trong hỗn hợp ban đầu.
Bài 9: Có hỗn hợp gồm NaI và NaBr. Hoà tan hỗn hợp vào nước rồi cho brôm dư vào dung dịch. Sau khi phản ứng thực hiện xong, làm bay hơi dung dịc làm khô sản phẩm, thì thấy khối lượng của sản phẩm nhỏ hơn khối lượng hỗn hợp 2 muối ban đầu là m(g). Lại hoà tan sản phẩm vào nước và cho clo lội qua cho đến dư, làm bay hơi dung dịch và làm khô, chất còn lại người ta thấy khối lượng chất thu được lại nhỏ hơn khối lượng muối phản ứng là m(g). Tính thành phần % theo khối lượng của NaBr trong hỗn hợp ban đầu.
Hướng dẫn:
Gọi a, b lần lượt là số mol của NaBr và NaI.
Khi sục Br2 vào trong dung dịch thì chỉ có NaI phản ứng và toàn bộ NaI chuyển thành NaBr. Vậy tổng số mol NaBr sau phản ứng (1) là: (a + b) mol.
Sau phản ứng (1) khối lượng giảm: m = mI – mBr = (127 – 80)b = 47b (*)
Tiếp tục sục Cl2 vào trong dung dịch thì chỉ có NaBr phản ứng và toàn bộ NaBr chuyển thành NaCl. Vậy tổng số mol NaCl sau phản ứng (2) là: (a + b) mol.
Sau phản ứng (2) khối lượng giảm: m = mBr – mCl = (80 – 35,5)(a + b) = 44,5(a + b) (**)
Từ (*) và (**) ta có: b = 17,8a
Vậy %mNaBr = (103a : (103a + 150b)) . 100% = 3,7%